Birbirine Karışmayan Sıvılar ve Karışmama Nedenleri
Bazı sıvılar birbirine karışmaz ve bu durum genellikle moleküler düzeydeki temel farklılıklardan kaynaklanır. Bu sıvılar, karıştırıldıklarında ayrı fazlar oluşturur ve birbirlerinden net bir şekilde ayrılırlar. İşte bu durumun arkasındaki başlıca nedenler ve yaygın örnekler:
Karışmamanın Temel Nedenleri
- Polarite Farklılıkları: Sıvıların molekülleri polar (kutuplu) veya polar olmayan (kutupsuz) yapıda olabilir. Polar moleküller, su gibi, pozitif ve negatif yük dağılımına sahiptir ve diğer polar maddelerle etkileşime girer. Polar olmayan moleküller ise, yağlar gibi, yük dağılımı eşit olduğu için polar sıvılarla karışmaz. "Benzer benzeri çözer" kuralına göre, polar sıvılar polar olanlarla, polar olmayan sıvılar ise polar olmayanlarla karışır.
- Yüzey Gerilimi ve Moleküler Çekim Kuvvetleri: Sıvıların yüzey gerilimi, molekülleri arasındaki çekim kuvvetlerinden kaynaklanır. Farklı sıvıların molekülleri arasındaki çekim kuvvetleri zayıf olduğunda, bir arada durmak yerine ayrılmaya meyillidirler. Örneğin, su molekülleri arasındaki güçlü hidrojen bağları, yağ moleküllerinin suya karışmasını engeller.
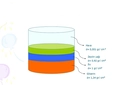
- Yoğunluk Farklılıkları: Karışmayan sıvılar genellikle farklı yoğunluklara sahiptir, bu da birinin diğerinin üzerinde veya altında toplanmasına neden olur. Yoğunluk, karışmama durumunu doğrudan belirlemez, ancak ayrışmayı kolaylaştırır.
- Dielektrik Sabit Farklılıkları: Sıvıların dielektrik sabitleri, polarizasyon yeteneklerini gösterir. Dielektrik sabitleri birbirinden çok farklı olan sıvılar (örneğin, su ve hidrokarbonlar) karışmaz, çünkü moleküler etkileşimler uyumsuzdur.
Yaygın Örnekler
- Su ve Yağ: En bilinen örneklerden biridir. Su polar, yağ ise polar olmayan (hidrofobik) yapıdadır. Karıştırıldıklarında, yağ suyun üzerinde bir tabaka oluşturur ve moleküler uyumsuzluk nedeniyle karışmazlar.
- Su ve Cıva: Cıva, metalik bir sıvıdır ve suyla karışmaz. Yoğunluğu çok yüksek olduğu için suyun altında toplanır ve polar olmayan yapısı suyun polaritesiyle uyumsuzdur.
- Su ve Benzin/Hekzan: Benzin gibi hidrokarbon bazlı sıvılar polar değildir ve suyla karışmaz. Bu, petrol sızıntılarında su yüzeyinde yağlı tabakalar oluşmasının nedenidir.
- Su ve Silikon Yağı: Silikon yağları genellikle polar olmayan yapıdadır ve suyla karışmaz, laboratuvarlarda ve endüstride yaygın olarak kullanılır.
- Alkol ve Yağ: Bazı alkoller (örneğin, etanol) suyla karışabilse de, yüksek polariteye sahip olmayan yağlarla karışmaz, çünkü moleküler çekim kuvvetleri yetersiz kalır.
Özet
Sıvıların karışmaması, temel olarak polarite, yüzey gerilimi ve moleküler etkileşim farklılıklarından kaynaklanır. Bu prensipler, kimya ve biyolojide emülsiyonlar, çözücü seçimi ve madde ayrıştırma gibi birçok uygulama için kritik öneme sahiptir. Günlük hayatta, salata sosları veya yağ-su karışımları gibi örneklerde bu durumu gözlemlemek mümkündür.
|






.webp)













.webp)