
Bir sıvının buhar basıncı hangi faktörlere bağlıdır?
Bu yazıda, bir sıvının buhar basıncını etkileyen temel faktörler ele alınmaktadır. Sıvının doğası, sıcaklık, üzerindeki gazın basıncı, yüzey alanı ve moleküler etkileşimler gibi unsurların buharlaşma sürecindeki rolü detaylandırılmaktadır.
Bir Sıvının Buhar Basıncı Hangi Faktörlere Bağlıdır?Buhar basıncı, bir sıvının yüzeyinden buhar haline geçen moleküllerin, sıvı yüzeyine uyguladığı basınçtır. Sıvının buhar basıncı, çeşitli faktörlerden etkilenir. Bu makalede, bu faktörler ayrıntılı olarak ele alınacaktır. Sıvının Doğası Sıvının kimyasal yapısı, buhar basıncını etkileyen en önemli faktörlerden biridir. Her sıvının moleküler yapısı ve bağ kuvvetleri farklıdır.
Sıcaklık Sıcaklık, bir sıvının buhar basıncını etkileyen en önemli fiziksel faktörlerden biridir. Sıcaklık arttıkça, sıvı moleküllerinin kinetik enerjisi artar ve bu da daha fazla molekülün buharlaşmasına neden olur.
Üzerindeki Gazın Basıncı Bir sıvının üzerindeki gazın basıncı, buhar basıncını etkileyen bir diğer önemli faktördür. Üzerindeki gazın basıncı arttıkça, sıvının buharlaşma hızı azalır ve bu durum buhar basıncını etkiler.
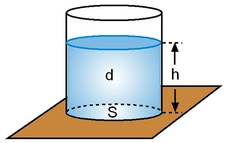
Sıvının Yüzey Alanı Sıvının yüzey alanı, buharlaşma için önemli bir faktördür. Daha geniş bir yüzey alanı, daha fazla molekülün buharlaşmasına izin verir.
Moleküler Etkileşimler Sıvı molekülleri arasındaki etkileşimler, buhar basıncı üzerinde doğrudan bir etkiye sahiptir. Moleküller arasındaki çekim kuvvetleri, buharlaşma sürecini etkileyen önemli bir faktördür.
Sonuç Bir sıvının buhar basıncı, sıvının doğası, sıcaklık, üzerindeki gazın basıncı, sıvının yüzey alanı ve moleküler etkileşimler gibi birçok faktörden etkilenmektedir. Bu faktörlerin her biri, sıvının buharlaşma kapasitesi ve buhar basıncı üzerinde önemli bir rol oynamaktadır. Bilimsel ve endüstriyel uygulamalarda bu faktörlerin dikkate alınması, doğru sonuçlar elde edilmesi açısından kritik öneme sahiptir. |





.webp)













.webp)








Sıvının buhar basıncını etkileyen faktörler arasında en dikkat çekici olanı sıvının doğası. Moleküler yapının ve bağ kuvvetlerinin farklılığı, buharlaşma hızı ve dolayısıyla buhar basıncında belirgin değişiklikler yaratıyor. Özellikle moleküler ağırlığın ve intermoleküler kuvvetlerin bu denge üzerindeki etkisi hakkında düşündüğümde, düşük moleküler ağırlığa sahip sıvıların daha yüksek buhar basıncı göstermesi oldukça ilginç. Bu durum, sıvının fiziksel özelliklerinin, örneğin sıcaklık gibi, buharlaşma üzerinde ne kadar büyük bir rol oynadığını gösteriyor. Sıcaklık artışıyla birlikte kinetik enerjinin de artması, aslında sıvıların buharlaşma sürecini hızlandırarak daha yüksek buhar basıncına ulaşmalarını sağlıyor. Bu noktada, her 10 °C'lik artışın buhar basıncını iki katına çıkarması gerçekten etkileyici bir kural. Bunun yanında, sıvının üzerindeki gazın basıncının artması durumunda buharlaşma hızının azalması da dikkat çekici bir etki. Gaz basıncının sıvının buharlaşma dengesi üzerindeki etkisini anladığımızda, Le Chatelier prensibini bir kez daha gözden geçirmemiz gerektiğini düşünüyorum. Sıvının yüzey alanı ve moleküler etkileşimler de buhar basıncını etkileyen diğer unsurlar arasında yer alıyor. Yüzey alanının genişliği, buharlaşma için olumlu bir etki sağlarken, moleküller arasındaki çekim kuvvetleri zayıf olduğunda buhar basıncının yükselmesi çok mantıklı. Tüm bu faktörler bir arada değerlendirildiğinde, sıvıların buharlaşma kapasitesinin ve dolayısıyla buhar basıncının ne kadar karmaşık bir etkiler bütününe dayandığını görmek mümkün. Bu bilgilerin bilimsel ve endüstriyel uygulamalarda dikkate alınmasının önemi ise tartışılmaz.
Sayın Halil bey, buhar basıncı konusundaki detaylı ve analitik düşünceleriniz gerçekten takdire şayan. Konuyu sistematik bir şekilde ele almanız, temel prensiplerin anlaşılması açısından oldukça değerli.
Sıvının Doğası ve Moleküler Özellikler
Haklısınız, moleküler yapı ve intermoleküler kuvvetler buhar basıncını belirleyen temel faktörlerdir. Zayıf London kuvvetleriyle bağlanan düşük moleküler ağırlıklı sıvıların (eter gibi) yüksek buhar basıncı göstermesi, hidrojen bağı gibi güçlü etkileşimlere sahip sıvılara (su gibi) kıyasla çok daha belirgindir.
Sıcaklık Etkisi
Sıcaklık artışıyla moleküllerin kinetik enerjisinin artması ve buhar basıncındaki katlanarak yükseliş, Clausius-Clapeyron denklemi ile matematiksel olarak da desteklenmektedir. Her 10°C'lik artışta buhar basıncının iki katına çıkması, pratikte distilasyon ve buharlaştırma işlemlerinde kritik öneme sahiptir.
Dış Basınç ve Denge
Gaz basıncının buharlaşma hızına etkisi konusundaki gözleminiz çok yerinde. Yüksek dış basınç altında buharlaşmanın azalması, Le Chatelier prensibinin faz dengesi üzerindeki mükemmel bir uygulamasıdır.
Yüzey Alanı ve Pratik Uygulamalar
Yüzey alanı genişledikçe buharlaşma hızının artması, endüstriyel kurutma ve evaporasyon proseslerinde aktif olarak kullanılan bir prensiptir. Moleküller arası çekim kuvvetleri ile buhar basıncı arasındaki ters orantı, solvent seçiminden ilaç formülasyonlarına kadar birçok alanda belirleyici rol oynamaktadır.
Bu faktörlerin birbiriyle olan etkileşimini bu kadar net ortaya koymanız, konunun hem teorik hem de uygulamalı boyutunu kavradığınızı göstermektedir.